Malaria, die Krankheit mit dem wunderschönen Namen „schlechte Luft“. Früher dachten die Menschen, dass die Erkrankung durch Miasma, also krankmachende Dämpfe, vor allem aus Sümpfen hervorgerufen wird, und ganz so weit weg von der Wahrheit war das gar nicht. Auch handelte es sich ursprünglich gar nicht um eine Tropenkrankheit: Malaria war über Jahrtausende hinweg Ursache für viele Todesfälle in Europa und verhinderte über lange Zeit den Zusammenbruch des Römischen Kaiserreiches. Na, wenn das mal keine krasse Einleitung ist. Seid ihr bereit für mehr?
Vom antiken Rom bis zur Juragewässerkorrektion
Falls jetzt der Gedanke aufkam, die Römer hätten Biowaffen genutzt, um ihre Feinde zu vernichten, so muss ich mich entschuldigen: Nein, natürlich taten sie das nicht.
Sie nutzten Biowaffen zur Verteidigung.
Oder besser gesagt, sie profitierten von der puren Existenz einer tödlichen Krankheit, die vor allem Italien regelmäßig heimsuchte. Die später als „mal’aria“ (schlechte Luft), bis dahin aber Wechselfieber genannte Krankheit, wütete zwar vor allem im Gebiet um die Pontinischen Sümpfe südöstlich von Rom, wurde jedoch in der Nähe vieler stehender Gewässer festgestellt. Diesem Umstand ist es mindestens zwei Mal zu verdanken, dass das Kaiserreich kein gotisches wurde. Zwar schafften es die Westgoten im August des Jahres 410, Rom zu erobern und zu plündern, aber kurz nach der Machtergreifung fielen König Alarich und hunderte seiner Soldaten einer heimtückischen Krankheit zum Opfer. Genauso erging es dem ostgotischen König Theoderich im August 526 in Ravenna.
Im Laufe der Jahrhunderte gab es viele prominente Opfer. Allein zwischen 1046 bis 1057 verstarben gleich vier deutsche Päpste hintereinander am tückischen Wechselfieber. Auch die Erkundung Afrikas durch Europäer fand mit Malariainfektionen immer wieder ein jähes Ende, festgehalten im zeitgenössischen Namen für die afrikanische Westküste: „Das Grab des weißen Mannes“. Erst im 18. Jahrhundert gelang es, die Krankheit zumindest teilweise zu bekämpfen. Quina, später Chinarinde genannt, wurde von südamerikanischen Jesuiten beschrieben und fand seinen weg als „Jesuitenpulver“ nach Europa. Das enthaltene Chinin ermöglichte im 19. Jahrhundert die Entdeckungsreisen in Afrika.
Die tatsächliche Ursache der Malaria war jedoch immer noch nicht bekannt. Entsprechend der vorherrschenden Säftelehre vermutete man bei ihr, wie auch bei der Pest, die Ursache in giftigen Dämpfen. Das war jedoch Grund genug für den Schweizer Arzt Johann Rudolf Schneider, im Berner Nationalrat für eine Korrektion der Gewässer im Jura zu werben; Das und natürlich auch der potentielle Gewinn von Flächen für die Landwirtschaft. Er war schließlich auch Politiker. Egal aus welchem Grund, nach der Korrektion trat Malaria immer seltener auf. Und nur wenige Jahre später (1880) konnte der französische Arzt Alphonse Laveran diesen Umstand erklären, als er den Erreger der Malaria unter dem Mikroskop ausfindig machte: kleine „fadenförmige Elemente, die Geißeln ähnelten, sich schnell bewegten […].“ Anfangs stieß seine Entdeckung auf Skepsis, aber mit der Unterstützung von Louis Pasteur erfuhr er noch im selben Jahrzehnt Anerkennung.
Die fadenförmigen Elemente und ihr Lebenszyklus
Anders als die meisten Infektionskrankheiten wird Malaria nicht durch Viren oder Bakterien ausgelöst, sondern durch Plasmodien, einzellige Parasiten, die den Menschen in ihrem Lebenszyklus als Zwischenwirt nutzen. Dieser lässt sich wie folgt beschreiben:
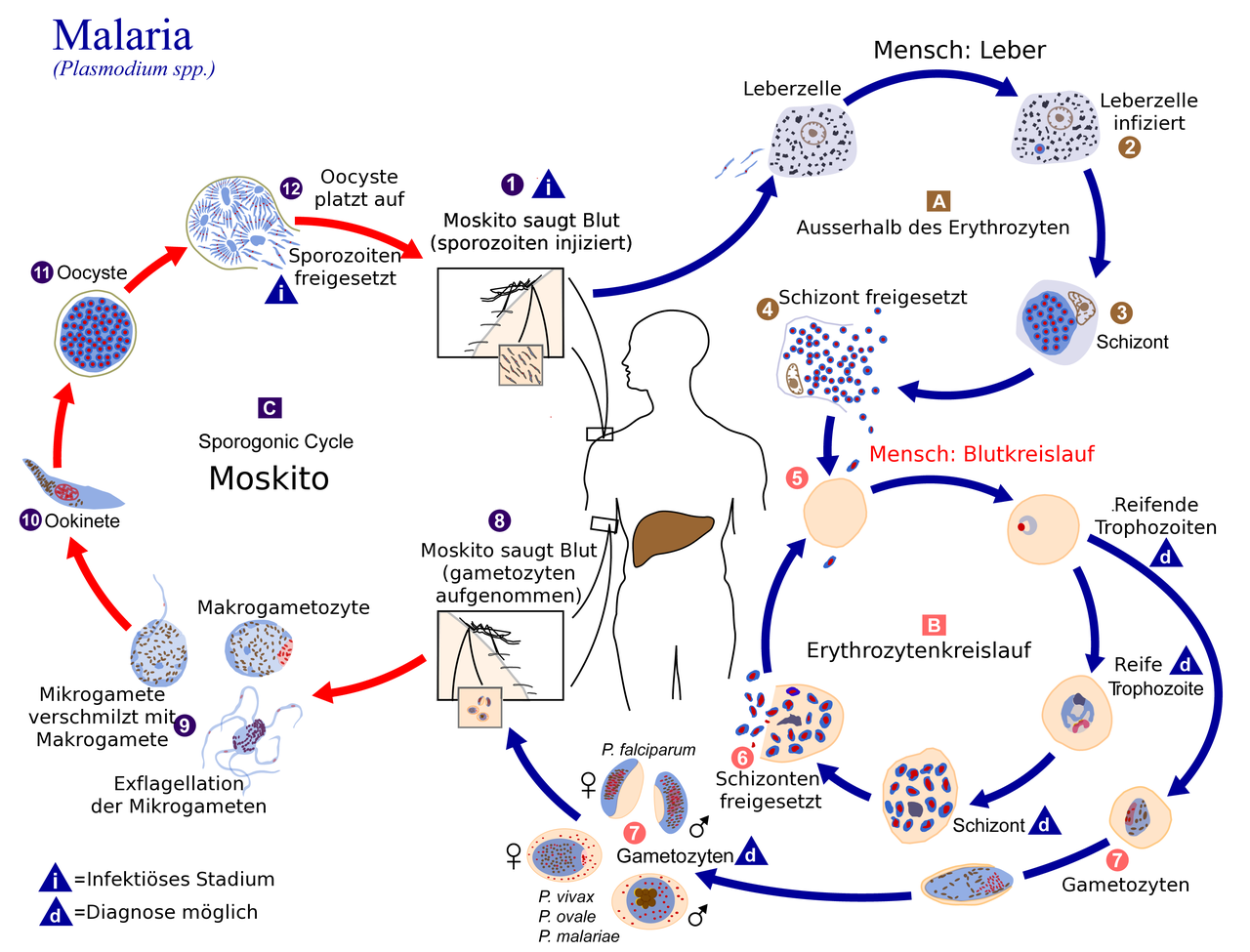
Sobald ein Moskito anfängt, Blut zu saugen, injiziert er auch Speichel, der neben Gerinnungshemmern (welche für das typische Jucken verantwortlich sind) auch hunderte Sporozoiten enthält (1). Diese wandern mit dem Blut bis zur Leber, wo sie Zellen infizieren (2) und dort zu einem Leberschizonten heranreifen, in welchem sie sich viele Male teilen (3). Der Schizont löst sich irgendwann auf und gibt mehrere tausend Merozoiten in die Blutbahn frei (4), welche wiederum in rote Blutkörperchen eindringen (5) und dort ihre nächste Reifephase beginnen. Diese ist aber zweigeteilt: Während die meisten Merozoiten in der Zelle zu einem Trophozoiten reifen, welcher wieder neue Merozoiten bildet, die weitere Blutkörperchen befallen (6), reift ein geringer Teil auch zu Gametozyten heran (7). Anders als bisher besitzt diese Form des Erregers verschiedene Geschlechter.
Wenn jetzt ein weiterer Moskito Blut saugt, nimmt er dabei diese Gametozyten auf (8), welche im Darm zu Mikro- und Makrogameten wachsen (9). Nach der Verschmelzung bildet sich ein Ookinet (10), reift zu einer Oozyste (11) und diese bildet dann neue Sporozoiten, die den nächsten Menschen befallen.
Die typischen Krankheitssymptome der Malaria treten zyklisch auf, und zwar immer dann, wenn die roten Blutkörperchen aufplatzen. Neben den Merozoiten werden dann nämlich auch Giftstoffe freigesetzt. Je länger die Erkrankung besteht, desto mehr Erreger befinden sich im Körper und desto mehr Toxine werden freigesetzt. Deshalb ist eine frühzeitige Behandlung auch so wichtig. Es gibt zwar verschiedene Erreger, die verschiedene Arten der Malaria auslösen, aber der Werdegang ist derselbe. Gelegentlich kommt es vor, dass entweder ungeteilte Erreger als Hypnozyt in der Leber verbleiben oder nur sehr wenige Blutzellen befallen werden. So können auch nach Jahrzehnten plötzlich Symptome auftreten. Eine Malaria kann in seltenen Fällen auch erst nach 50 Jahren ausbrechen.
Eine Impfung ist in Sicht
Aufgrund des komplizierten Lebenszyklus der Plasmodien in Moskito, Leber und Blutkreislauf sowie ihrer Anpassungsfähigkeit und Größe war es bislang unmöglich, einen wirksamen Impfstoff herzustellen. Bisher zumindest. Nach 30 Jahren Forschung startete 2019 ein großangelegter Versuch mit dem von GSK entwickelten Impfstoff RTS,S/AS01. Zur besseren Aussprache wurde der Markenname Mosquirix gewählt. Es handelt sich um einen Totimpfstoff, den weltweit ersten Impfstoff gegen einen Parasiten überhaupt, der das Immunsystem trainiert, die Erreger auf dem Weg zur Leber und dort als während des Übergangs zum Schizonten anzugreifen. In drei Jahren der letzten Versuchsphase konnten beeindruckende Ergebnisse erzielt werden, die für uns wohlstandsverwöhnte Europäer erstmal gar nicht so toll klingen.
In Ghana, Kenia und Malawi wurden 800.000 Kinder damit geimpft, was drei Impfdosen zur Grundimmunisierung beinhaltet sowie einen Booster nach maximal zwei Jahren. Ohne nennenswerte Nebenwirkungen und ohne den übrigen Impfplan zu beeinflussen, wurden nach vier Jahren ein Rückgang der Malariatodesfälle bei Kindern um 13% sowie eine 22%ige Reduktion schwerer Verläufe bei Kindern festgestellt. Das klingt nach gar nicht so viel. Bedenkt man aber, dass die Gesundheitssysteme der drei Ländern mangelhaft und chronisch unterversorgt sind und weltweit jedes Jahr eine halbe Million Kinder an Malaria und deren Folgen verstirbt, sind das fantastische Neuigkeiten. Eine Impfstoffdosis kostet umgerechnet nicht einmal 10€, weshalb Mosquirix problemlos in das bestehende Impfschema integriert werden kann. Leider ist er nicht so leicht zu produzieren: bis 2025 stehen voraussichtlich nur 18 Millionen Einheiten zur Verfügung. Viel zu wenig für eine flächendeckende Verteilung.
Doch Rettung naht: Anfang Oktober 2023 wurden die ersten Ergebnisse eines Versuchs mit einem anderen Impfstoff von Novavax bekannt gegeben. Während Mosquirix vermutlich bis zu 30% der schweren Verläufe und daraus resultierender Todesfälle verhindern wird, schützt R21/Matrix-M zu 80% vor einer Infektion der Blutzellen, welche die eigentlich Krankheit auslöst. Die Präqualifikation durch die WHO steht noch aus, doch mit einer flächendeckenden Verteilung wird bis Mitte 2024 gerechnet. Ein weiterer Vorteil liegt in den Kosten: Eine Impfdosis kostet nicht einmal 2€. Insgesamt geht die WHO davon aus, dass mit diesen beiden Impfstoffen die Kindersterblichkeit in Malariagebieten um bis zu 50% reduziert werden kann.
Ein Ausblick
Zugegeben, das sind tatsächlich mal sehr positive Nachrichten. On top gibt es aber noch eine ganz andere Entwicklung. Nicht nur als Impfstoff, sondern auch zur akuten Behandlung wird gerade an Mitteln mit dem Gen UIS3 geforscht. Dieses bildet ein membranspezifisches Protein der Sporozoiten. Wird dieses Gen gezielt blockiert, ist es den Plasmodien nicht mehr möglich, in den roten Blutkörperchen eine Umwandlung zu Geschlechtszellen zu vollziehen. Das klingt nicht nur nach einem Geniestreich: Auf lange Sicht würde dieses Verfahren nicht nur Erkrankungen drastisch reduzieren, sondern auch die genetische Vielfalt der Erreger. Aufgrund der schnellen Reproduktionsrate der Plasmodien wären die Auswirkungen bereits innerhalb weniger Jahrzehnte zu spüren.
Der einzige Wermutstropfen ist, dass keiner der verfügbaren Impfstoffe für Reisende aus anderen Ländern angedacht ist. Wollt ihr also in Malariagebiete reisen, so braucht ihr weiterhin die typischen Mittelchen wie Insektenspray und Moskitonetze, um euch vor der Krankheit zu schützen.
Noch.
Eure Enkelkinder schützen sich vielleicht schon nur noch vor dem lästigen Juckreiz.
Quellen
https://www.planet-wissen.de/gesellschaft/krankheiten/malaria/pwiegeschichtedermalaria100.html
https://www.deutschlandfunk.de/epidemiologie-vor-140-jahren-entdeckte-alphonse-laveran-den-100.html
https://flexikon.doccheck.com/de/Malaria
https://de.wikipedia.org/wiki/Malaria
https://de.wikipedia.org/wiki/Malariaimpfstoff
https://www.science.org/content/article/first-malaria-vaccine-slashes-early-childhood-deaths
https://www.gelbe-liste.de/nachrichten/neuer-malaria-impfstoff-klinische-studie